Bölüm
3 - Radyasyon "Radyasyon ve Biz" |
| 1
Temel Bilgiler |
1.1 Atom
Canlı veya
cansız tüm varlıklar atomlardan oluşurlar. Yetişkin bir insan
vücudunu, yaklaşık 4x1027 oksijen, karbon, hidrojen,
nitrojen, fosfor, potasyum, ve diğer elementlerin atomlarının
oluşturduğu bir paket gibi düşünebiliriz [1,2].
Bir elementin
tüm kimyasal özelliklerine sahip en küçük parçası olan atom; proton,
nötron ve elektronlardan oluşur (Şekil 1.1). Çapı, yaklaşık olarak
10-10 metre olan atomun belli bir kütlesi vardır ve
bu kütlenin neredeyse tamamı, kendi hacminin yaklaşık olarak 1015
de biri kadar hacime sahip çekirdeğinde yoğunlaşmıştır [3,4,5].
|
1.2 İzotop

Proton sayıları
aynı, ancak nötron sayıları farklı olan atom çekirdeklerine izotop
denir. Bir elementin farklı sayılarda izotopları olabilir. Bu
izotoplar, nötron sayıları farklı olduğundan, farklı kütle numaralarına
sahiptirler. Örneğin, Hidrojen elementinin 3 izotopu vardır (Şekil
1.2). Bir elementin bütün izotopları aynı kimyasal özellikleri
gösterir. Ancak fiziksel özellikleri farklıdır.
1.3
İyonizasyon
Herhangi
bir nedenden dolayı atomdan bir elektron kopartılması veya atoma
bir elektron bağlanması sonucunda atomun yük dengesi bozulur (Şekil
1.3). Bu olaylara iyonizasyon,
iyonizasyon sonucu oluşan atoma iyon
denir.
|
1.4
Radyoaktivite
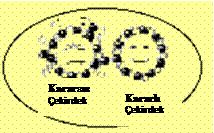 Doğada
mevcut elementlerin atomlarının bir kısmı kararlı diğer
bir kısmı ise kararsız çekirdeklere sahiptirler. Kararlı
bir çekirdekte, çoğu durumda nötron sayısı (N) proton sayısından
(Z) biraz daha yüksek ve N/Z oranı yaklaşık olarak 1,50 civarındadır.
Kararlı bir çekirdekte, proton ve nötronlar birbirlerine nükleer
kuvvetlerle o kadar sıkı bağlıdırlar ki hiçbir parçacık çekirdek
dışına kaçamaz. Bu durumda, çekirdek dengede kalacaktır. Ancak,
çekirdek dengede değilse yani kararsız ise, fazla bir enerjiye
sahip olacak ve parçacıkları bir arada kalamayacaktır. Kısa bir
süre içinde veya daha uzun bir süre sonra bu fazla enerjisini
boşaltacaktır. En basit
çekirdek olan Hidrojen (H) çekirdeğinin dışındaki tüm çekirdekler
nötron ve protonlardan oluşmuştur. N/Z oranı hafif izotoplarda
1 iken, ağır çekirdeklere doğru gidildikçe bu oran artmaktadır.
Bu oran arttıkça çekirdeklerin artık kararlı olmadığı bir yere
ulaşılır. En ağır kararlı çekirdek bir bizmut izotopudur (Bi-207).
Daha ağır çekirdekler sahip oldukları fazla enerjiden dolayı kararsızdırlar.
Böyle çekirdeklere radyoaktif çekirdek veya radyoizotop adı verilir.
Bunlar fazla enerjilerinden kurtulmaya ve kararlı duruma geçmeye
çalışırlar. Bu olaya radyoaktivite veya radyoaktif parçalanma
denir.Radyoaktivite kontrol edilemeyen bir olaydır. Herhangi bir
şekilde müdahale edilip yavaşlatılamaz veya durdurulamaz. Üstel
bir fonksiyon şeklindeki zayıflayan bir tempo ile azalarak kendiliğinden
tükeninceye kadar devam eder. Radyoaktivite olayı doğal
ve yapay olarak iki farklı şekilde meydana gelebilir.Doğada
mevcut bulunan kararsız elementler kararlı yapıya geçmeye çalışırken,
hiçbir dış müdahale olmadan, sahip oldukları fazla enerjilerini
çekirdeklerinden dışarı salarlar. Böyle elementlere doğal radyoaktif
elementler, bunların enerji salma olayına da doğal radyoaktivite
denir. Doğada kararlı olarak bulunan izotoplar da yapay yollarla
kararsız (radyoaktif) hale getirilebilirler. Radyoaktif hale gelen
çekirdek parçalanmaya uğrar. Bu olay yapay radyoaktivite olarak
adlandırılır. Doğada
mevcut elementlerin atomlarının bir kısmı kararlı diğer
bir kısmı ise kararsız çekirdeklere sahiptirler. Kararlı
bir çekirdekte, çoğu durumda nötron sayısı (N) proton sayısından
(Z) biraz daha yüksek ve N/Z oranı yaklaşık olarak 1,50 civarındadır.
Kararlı bir çekirdekte, proton ve nötronlar birbirlerine nükleer
kuvvetlerle o kadar sıkı bağlıdırlar ki hiçbir parçacık çekirdek
dışına kaçamaz. Bu durumda, çekirdek dengede kalacaktır. Ancak,
çekirdek dengede değilse yani kararsız ise, fazla bir enerjiye
sahip olacak ve parçacıkları bir arada kalamayacaktır. Kısa bir
süre içinde veya daha uzun bir süre sonra bu fazla enerjisini
boşaltacaktır. En basit
çekirdek olan Hidrojen (H) çekirdeğinin dışındaki tüm çekirdekler
nötron ve protonlardan oluşmuştur. N/Z oranı hafif izotoplarda
1 iken, ağır çekirdeklere doğru gidildikçe bu oran artmaktadır.
Bu oran arttıkça çekirdeklerin artık kararlı olmadığı bir yere
ulaşılır. En ağır kararlı çekirdek bir bizmut izotopudur (Bi-207).
Daha ağır çekirdekler sahip oldukları fazla enerjiden dolayı kararsızdırlar.
Böyle çekirdeklere radyoaktif çekirdek veya radyoizotop adı verilir.
Bunlar fazla enerjilerinden kurtulmaya ve kararlı duruma geçmeye
çalışırlar. Bu olaya radyoaktivite veya radyoaktif parçalanma
denir.Radyoaktivite kontrol edilemeyen bir olaydır. Herhangi bir
şekilde müdahale edilip yavaşlatılamaz veya durdurulamaz. Üstel
bir fonksiyon şeklindeki zayıflayan bir tempo ile azalarak kendiliğinden
tükeninceye kadar devam eder. Radyoaktivite olayı doğal
ve yapay olarak iki farklı şekilde meydana gelebilir.Doğada
mevcut bulunan kararsız elementler kararlı yapıya geçmeye çalışırken,
hiçbir dış müdahale olmadan, sahip oldukları fazla enerjilerini
çekirdeklerinden dışarı salarlar. Böyle elementlere doğal radyoaktif
elementler, bunların enerji salma olayına da doğal radyoaktivite
denir. Doğada kararlı olarak bulunan izotoplar da yapay yollarla
kararsız (radyoaktif) hale getirilebilirler. Radyoaktif hale gelen
çekirdek parçalanmaya uğrar. Bu olay yapay radyoaktivite olarak
adlandırılır.
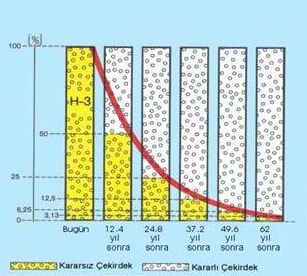 |
Şekil
1.4 Trityum radyoizotopunun yarılanma eğrisi |
Radyoizotopun aktivitesi, bir yarılanma süresi sonra
başlangıç aktivitesinin yarısına, iki yarılanma süresi sonra
başlangıç aktivitesinin dörtte birine (1/2x1/2=1/4), üç yarılanma
süresi sonra ise başlangıç aktivitesinin sekizde birine (1/2x1/2x1/2=1/8)
iner. Bu azalma, n
yarılanma süresi sayısı olmak üzere 1/2n
şeklinde devam eder. On yarılanma süresi sonra radyoizotopun
aktivitesi başlangıç aktivitesinin 1/210 ‘u kadar
olacaktır. Pratikte 7 veya 8 yarı ömür sonra bir radyoizotopun
aktivitesinin tamamen sona erdiği düşünülse de teoride aktivitenin
tükenene kadar sonsuza dek aynı hızla azalarak devam ettiği
varsayılır. Şekil 1.4 de, örnek olarak, başlangıçta
100 radyoaktif çekirdeğe sahip olan bir Trityum(H3)
radyoizotopun bozunum eğrisi gösterilmektedir. Trityum'un
yarılanma süresi 12.4 yıldır. 12.4 yılın sonunda bu radyoaktif
çekirdek sayısı elliye düşecektir. İkinci 12.4 yılın sonunda
ise bu sayı 25 olacak ve radyoaktif çekirdek sayısındaki azalma
(radyoizotopun aktivitesindeki azalma) bu şekilde devam edecektir.
Her radyoizotopun kendine özgü bir yarılanma süresi olduğunu
daha önce belirtmiştik. Örneğin yarılanma süresi 5.3 yıldır.
Başlangıçta 100 birim
aktiviteye sahip bir Co60 radyoizotopunun 5.3 yıl
sonraki aktivitesi 50 birime, 10.6 yıl sonraki aktivitesi
25 birime, 15.9 yıl sonraki aktivitesi 12.5 birime düşecek
ve düşüş bu şekilde devam edecektir.
Radyoizotopların
yarılanma süresini bilmek birçok durumda büyük önem taşır. Örneğin,
en son 2-3 ay önce kullanılarak muhafaza altına alınmış yarılanma
süresi 75 gün olan bir İridyum radyoizotopunun (Ir192)
aktivitesinin geçen bu 2-3 aylık zaman içerisinde yarıya indiğini
herhangi bir ölçüm yapmadan bilebiliriz. Detektör de bu değeri
gösteriyorsa her şey yolunda demektir.Ancak, muhafaza altındaki
izotop Ir192 değil de Co60 olmuş olsa
ve detektörde okunan değer 2-3 ay önce okunan değerin yarsını
gösteriyor olsa idi, o zaman bir sorunla karşı karşıya olduğumuz
sonucuna varırdık. Bu durumda, ilk olarak, ya
cihazımızın doğru çalışmadığı veya Co60 radyoizotopunun
muhafaza altına alındığı kap içerisinde bulunmadığına ya
da kap içerisinde başka bir radyoizotop bulunduğuna karar verirdik.
|
|
İçindekiler |
Bölüm
1 2
3 4
5 6
7
8 |
<
Geri |
İleri
> |
Kapat |
|





